Sesium klorida

| |
| |
| Nama | |
|---|---|
| Nama IUPAC
Sesium klorida
| |
| Nama lain
Sesium klorida
| |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChemSpider | |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| CsCl | |
| Massa molar | 168.36 g/mol |
| Penampilan | padat putih higroskopik |
| Densitas | 3.988 g/cm3[1] |
| Titik lebur | 646 °C (1.195 °F; 919 K)[1] |
| Titik didih | 1.297 °C (2.367 °F; 1.570 K)[1] |
| 1910 g/L (25 °C)[1] | |
| Kelarutan | Dapat larut dalam etanol[1] |
| Celah pita | 8.35 eV (80 K)[2] |
| -56.7·10−6 cm3/mol[3] | |
| Indeks bias (nD) | 1.712 (0.3 µm) 1.640 (0.59 µm) 1.631 (0.75 µm) 1.626 (1 µm) 1.616 (5 µm) 1.563 (20 µm)[4] |
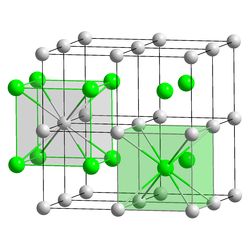
| Struktur | |
| CsCl, cP2 | |
| Pm3m, No. 221[5] | |
a = 0.4119 nm
| |
Volum kisi (V)
|
0.0699 nm3 |
Satuan formula (Z)
|
1 |
| Kubik (Cs+) Kubik (Cl−) | |
| Bahaya | |
| Dosis atau konsentrasi letal (LD, LC): | |
LD50 (dosis median)
|
2600 mg/kg (oral, rat)[6] |
| Senyawa terkait | |
Anion lain
|
Sesium fluorida Sesium bromida Sesium iodida Sesium astatida |
Kation lainnya
|
Litium klorida Natium klorida Kalium klorida Rubidium klorida Fransium klorida |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Sesium klorida adalah senyawa anorganik dengan rumus CsCl. Senyawa padat tidak berwarna ini merupakan sumber ion sesium yang penting. Senyawa ini dapat larut di dalam air dan dapat ditemui secara alami sebagai ketidakmurnian dalam mineral karnalit (hingga 0,002%), silvit dan kainit. Kurang dari 20 ton CsCl diproduksi setiap tahunnya di seluruh dunia, kebanyakan dari mineral polusit yang mengandung sesium.[7]
Sesium klorida sering digunakan dalam proses sentrifugasi isopiknik untuk memisahkan berbagai jenis DNA. Senyawa ini juga merupakan sebuah reagen dalam kimia analitis yang dimanfaatkan untuk mengenali ion dari warna dan morfologi endapannya. Jika diperkaya dengan radioisotop (seperti 137CsCl atau 131CsCl), sesium klorida dipakai dalam bidang kedokteran nuklir, seperti dalam penanganan kanker dan diagnosis infarksi miokardial.
Sesium klorida memiliki kadar racun yang rendah untuk manusia dan hewan, tetapi bentuk radioaktifnya dapat dengan mudah mencemari lingkungan karena CsCl mudah larut dalam air. Penyebaran bubuk 137CsCl dari wadah 93-gram pada tahun 1987 di Goiânia, Brasil, memicu salah satu peristiwa kebocoran radiasi terburuk yang menewaskan empat orang dan berdampak terhadap lebih dari 100.000 orang.
Pembuatan
Di bidang industri, CsCl dibuat dari mineral polusit. Ekstraknya direaksikan dengan antimon triklorida, iodin monoklorida atau serium(IV) klorida untuk memperoleh garam yang sulit larut:[8]
- CsCl + SbCl3 → CsSbCl4
Reaksi garam ini dengan hidrogen sulfida akan menghasilkan CsCl:[8]
- 2 CsSbCl4 + 3 H2S → 2 CsCl + Sb2S3 + 8 HCl
Catatan kaki
- ^ a b c d e Haynes, hlm. 4.57
- ^ Lushchik, A; Feldbach, E; Frorip, A; Ibragimov, K; Kuusmann, I; Lushchik, C (1994). "Relaxation of excitons in wide-gap CsCl crystals". Journal of Physics: Condensed Matter. 6 (12): 2357–2366. doi:10.1088/0953-8984/6/12/009.
- ^ Haynes, p. 4.132
- ^ Haynes, hlm. 10.240
- ^ Watanabe, M.; Tokonami, M.; Morimoto, N. (1977). "The transition mechanism between the CsCl-type and NaCl-type structures in CsCl". Acta Crystallographica Section A. 33 (2): 294. doi:10.1107/S0567739477000722.
- ^ Cesium chloride. nlm.nih.gov
- ^ Greenwood, Norman N.; Earnshaw, A. (1997), Chemistry of the Elements (Edisi 2), Oxford: Butterworth-Heinemann, ISBN 0-7506-3365-4 Pemeliharaan CS1: Banyak nama: authors list (link)
- ^ a b "Cesium and Cesium Compounds". Kirk-Othmer Encyclopedia of Chemical Technology. Vol. 5 (Edisi 4th). New York: John Wiley & Sons. 1994. hlm. 375–376.
Daftar pustaka
- Haynes, William M., ed. (2011). CRC Handbook of Chemistry and Physics (Edisi 92). Boca Raton, FL: CRC Press. ISBN 1439855110.
- Lidin, R. A; Andreeva, L. L.; Molochko V. A. (2006). Константы неорганических веществ: справочник (Inorganic compounds: data book). Moscow. ISBN 5-7107-8085-5. Pemeliharaan CS1: Lokasi tanpa penerbit (link)
- Plyushev, V. E.; Stepin B. D. (1970). Химия и технология соединений лития, рубидия и цезия (dalam bahasa Russian). Moscow: Khimiya. Pemeliharaan CS1: Bahasa yang tidak diketahui (link)

