Renium(IV) oksida

| |
 | |
| Nama | |
|---|---|
| Nama IUPAC
Renium(IV) oksida
| |
| Nama lain
Renium dioksida
| |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChemSpider | |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| ReO2 | |
| Massa molar | 218,206 g/mol |
| Penampilan | Kristal ortorombik berwarna abu-abu |
| Densitas | 11,4 g/cm3[1] |
| Titik lebur | Terdekomposisi pada suhu 1000 °C[2] |
| Tak larut | |
| Kelarutan dalam alkali | Tak larut |
| +44,0·10−6 cm3/mol | |
| Struktur | |
| Ortorombik, oP12 | |
| Pbcn, No. 60 | |
| Bahaya | |
| Lembar data keselamatan | MSDS Aldrich |
| Senyawa terkait | |
Anion lain
|
Renium(III) oksida Renium(VII) oksida Renium(III) klorida |
Kation lainnya
|
Mangan(IV) oksida Teknesium(IV) oksida |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
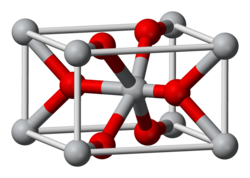
Renium(IV) oksida atau renium dioksida adalah sebuah senyawa anorganik dengan rumus kimia ReO2. Padatan kristalin berwarna abu-abu hingga hitam ini merupakan reagen laboratorium yang dapat digunakan sebagai katalis. Senyawa ini mengadopsi struktur rutil.
Sintesis dan reaksi
Senyawa ini terbentuk melalui komproporsionasi:[3]
- 2 Re2O7 + 3 Re → 7 ReO2
Kristal tunggal diperoleh melalui transpor kimia, menggunakan iodin sebagai agen transpor:[4]
- ReO2 + I2 ⇌ ReO2I2
Pada suhu tinggi, senyawa ini mengalami disproporsionasi:
- 7 ReO2 → 2 Re2O7 + 3 Re
Senyawa ini membentuk renat dengan hidrogen peroksida alkali dan asam oksidator.[5] Dalam leburan natrium hidroksida, senyawa ini membentuk natrium renat:[6]
- 2 NaOH + ReO2 → Na2ReO3 + H2O
Referensi
- ^ Lide, David R. (1998). Handbook of Chemistry and Physics (Edisi 87). CRC Press. hlm. 484. ISBN 0-8493-0594-2. Diakses tanggal 9 Juli 2025.
- ^ Perry, Dale L.; Phillips, Sidney L. (1995). Handbook of Inorganic Compounds. San Diego: CRC Press. hlm. 328. ISBN 0-8493-8671-3. Diakses tanggal 9 Juli 2025.
- ^ G. Glemser "Rhenium (IV) Oxide" Handbook of Preparative Inorganic Chemistry, 2nd Ed. Disunting oleh G. Brauer, Academic Press, 1963, NY. Vol. 1. hlm. 1480.
- ^ Rogers, D. B.; Butler, S. R.; Shannon, R. D. (1972). "Single Crystals of Transition-Metal Dioxides". Inorganic Syntheses. Vol. XIII. Wiley. hlm. 135–145. doi:10.1002/9780470132449.ch27. ISBN 9780470131725.
- ^ "RHENIUM DIOXIDE - Manufacturer". Aaamolybdenum.com. Diarsipkan dari asli tanggal 9 Februari 2003. Diakses tanggal 9 Juli 2025.
- ^ G. Glemser "Sodium Rhenate (IV)" Handbook of Preparative Inorganic Chemistry, 2nd Ed. Disunting oleh G. Brauer, Academic Press, 1963, NY. Vol. 1. hlm. 1483.

